Assaisonné par la science : la chimie des épices
Assaisonné par la science : la chimie des épices
par Gay Wilson
La Semaine nationale de la chimie est célébrée chaque octobre. Le thème de cette année est La vie cachée des épices. C’est une excellente occasion d’explorer la science moléculaire des épices avec la chimie de Wolfram.
Mélange d’épices à la citrouille
Mélange d’épices à la citrouille
L’automne est arrivé, et le parfum de citrouille épicée fait son apparition saisonnière dans les cafés, les pâtisseries et même dans les friandises pour nos compagnons à quatre pattes. Il est possible de personnaliser les mélanges d’épices à la citrouille avec une variété d’épices réchauffantes, mais une chose est certaine dans tous les cas : il n’y a pas de citrouille !
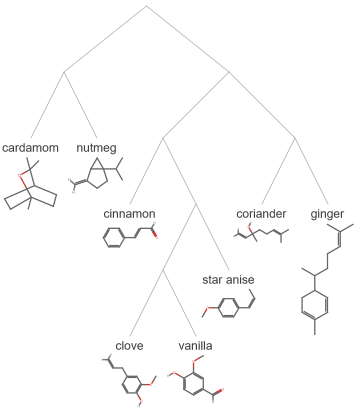
Avec la fonction MoleculeFeatureDistance, également appelée distance d’empreinte moléculaire, vous pouvez calculer la dissimilarité entre deux molécules. Sur une échelle de 0 à 1, une distance plus petite indique une plus grande similarité ; une distance plus grande indique une dissimilarité plus grande.
In[]:=
pumpkinSpiceBlendAssoc=<|"cardamom"->,"cinnamon"->,"clove"->,"coriander"->,"ginger"->,"nutmeg"->,"star anise"->,"vanilla"->|>;tree=ClusteringTree[pumpkinSpiceBlendAssoc,DistanceFunction->MoleculeFeatureDistance];labels=AnnotationValue[tree,"LeafLabels"];vertexLabels=Lookup[AbsoluteOptions[tree],VertexLabels]/.{s_StringMoleculePlot[pumpkinSpiceBlendAssoc[s],PlotLabels,ImageSize60],CenterBelow};Graph[tree,VertexLabels->vertexLabels,ImageSize->Medium]
Out[]=
Monoterpènes
Monoterpènes
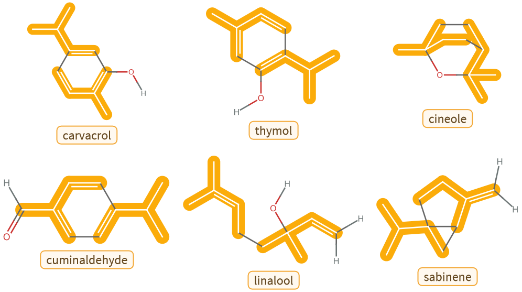
Beaucoup de nos épices préférées présentent des monoterpènes ou des monoterpénoïdes dans leur structure chimique, notamment l’origan (carvacrol), le thym (thymol), la cardamome et le romarin (cinéole), le cumin (aldéhyde cuminique), la coriandre (linalol) et la noix de muscade (sabinéne).
En plus d’apporter des arômes et des saveurs délicieux, qu’ont en commun ces molécules ? Dix atomes de carbone et deux unités d’isoprène, visualisés avec Wolfram Language.
In[]:=
monoterpenePattern=MoleculePattern["[#6]~[#6](~[#6])~[#6]~[#6].[#6]~[#6](~[#6])~[#6]~[#6]"];Labeled[MoleculePlot[Molecule[#],monoterpenePattern,AtomDiagramCoordinates->"OpenBabel"],#]&/@,,,,,//Partition[#,3]&//Grid
Out[]=
Structure commune de la moutarde forte, du wasabi et du raifort
Structure commune de la moutarde forte, du wasabi et du raifort
Vous connaissez cette sensation de brûlure soudaine dans le nez quand vous mangez de la moutarde forte, du wasabi ou du raifort ?
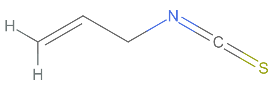
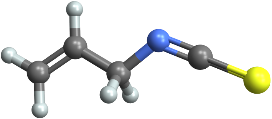
Cette sensation est due au groupe isothiocyanate (R−N=C=S), hautement volatil et réactif, présent dans l’isothiocyanate d’allyle (AITC). L’AITC est libéré lorsque nous brisons les cellules des graines de moutarde, du wasabi et du raifort en les coupant, les râpant ou les mâchant.
La sensation s’estompe rapidement ; juste à temps pour votre prochaine bouchée !
In[]:=
MoleculePlot
Out[]=
In[]:=
MoleculePlot3D
Out[]=
Isomères de l’origan et du thym
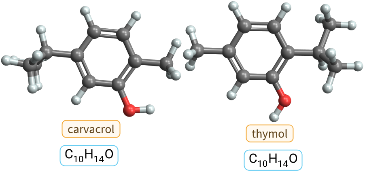
Isomères de l’origan et du thym
Nous aimons l’arôme de l’origan dans notre sauce pour les pâtes et la saveur terreuse du thym qui parfume notre poulet rôti et nos carottes glacées.
Les composés monoterpénoïdes de l’origan et du thym, le carvacrol et le thymol, sont des isomères phénoliques. Ils possèdent la même formule moléculaire, mais diffèrent par leur organisation structurelle.
Ils forment un excellent duo en cuisine et en chimie !
In[]:=
Labeled[MoleculePlot3D[#,ImageSize->Small],Column[{#,Molecule[#]["ChemicalFormula"]}]]&/@,//Row
Out[]=
Couleurs du curcuma, du safran et du paprika
Couleurs du curcuma, du safran et du paprika
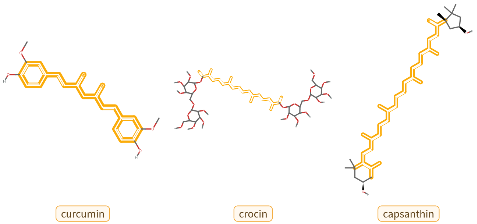
Qu’est-ce qui donne aux épices curcuma, safran et paprika leurs couleurs vives ? C’est leur structure moléculaire.
Lorsqu’une molécule possède un système conjugué de liaisons simples et doubles alternées, elle peut absorber l’énergie de la lumière visible.
La curcumine absorbe principalement la lumière bleue, ce qui donne au curcuma son apparence jaune. Les molécules de crocine absorbent la lumière bleu-violet, ce qui donne au safran sa couleur orange-rouge. La capsanthine absorbe la lumière bleu-vert, conférant au paprika une couleur rouge intense.
In[]:=
colorfulSpicesAssoc=<|"turmeric"->,"saffron"->,"paprika"->|>;KeyValueMap[{MoleculePlot[#2,{{MoleculePattern["[#6]:[#6]"],MoleculePattern["[#6]-[#6]=[#6,#8]"]}}],#2}&,colorfulSpicesAssoc]//Thread//Grid
Out[]=
La couleur, l’arôme et la saveur du safran
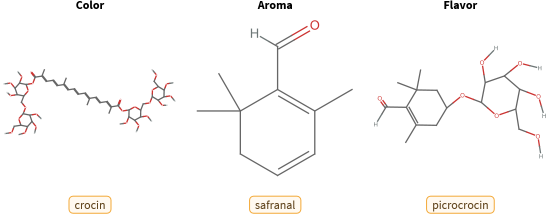
La couleur, l’arôme et la saveur du safran
En tant qu’épice la plus chère au monde, le safran est souvent appelé « l’or rouge ».
Quelles sont les molécules qui produisent la couleur, l’arôme et la saveur de cette précieuse denrée ?
Quelles sont les molécules qui produisent la couleur, l’arôme et la saveur de cette précieuse denrée ?
Le caroténoïde crocine constitue environ 80 % de la composition chimique du safran et est responsable de sa couleur jaune-orangé à rouge. Le safranal, présent dans son huile essentielle, donne au safran son arôme, et la picrocrocine est responsable de la saveur terreuse et amère du safran.
In[]:=
KeyValueMap{Style[Capitalize[#1],"Text",Medium,Bold],MoleculePlot[Molecule[#2],ImageSize->Small],#2}&,<|"color"->,"aroma"->,"flavor"->|>//Thread//Grid
Out[]=
Les senteurs des fêtes
Les senteurs des fêtes
La saison des repas festifs approche. Le monoterpénoïde cinéole, également connu sous le nom d’eucalyptol en raison de sa présence dans les huiles essentielles des arbres d’eucalyptus, est responsable de certains de nos arômes préférés de la période des fêtes : le romarin, le basilic doux, la cardamome, la feuille de laurier et la sauge. Vivement que la dinde et la farce arrivent !
CITER CE NOTEBOOK
CITER CE NOTEBOOK
Assaisonné par la science : la chimie des épices
par Gay Wilson
Communauté Wolfram, CHOIX DE L’ÉQUIPE, 24 octobre 2025
https://community.wolfram.com/groups/-/m/t/3564888
par Gay Wilson
Communauté Wolfram, CHOIX DE L’ÉQUIPE, 24 octobre 2025
https://community.wolfram.com/groups/-/m/t/3564888